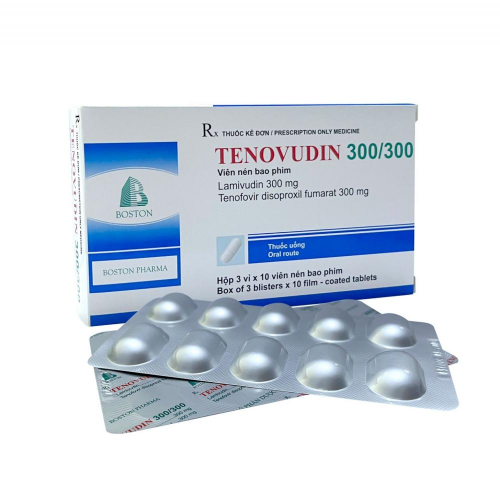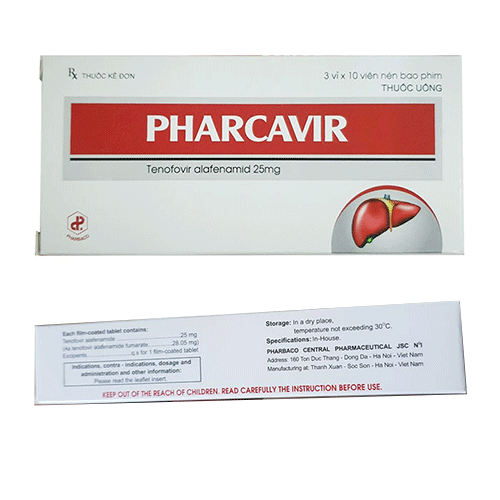
Pharcavir 25mg là thuốc gì, giá bao nhiêu mua ở đâu uy tín
Thuốc Pharcavir 25mg giá bao nhiêu rẻ nhất mua ở đâu hà nội? Thuốc Pharcavir 25mg là thuốc điều trị viêm gan B mạn tính với tác dụng là ức chế sự phát triển của virus viêm gan B HBV giúp bệnh nhân giảm tải lượng virus và sinh ra kháng thể để chống lại nó. Thuốc Pharcavir 25mg có chứa thành phần chính Tenofovir alafenamide 25mg là một chất ức chế mạnh quá trình sao chép ngược ADN để điều trị viêm gan B mạn tính và hỗ trợ điều trị nhiễm HIV, thuốc do công ty Dược phẩm Trung ương I – Pharbaco sản xuất. Hiện nay, trên thị trường có rất nhiều loại thuốc điều trị viêm gan B mãn tính. Tuy nhiên, mỗi tình trạng và bệnh nền của bệnh nhân sẽ phù hợp với những loại thuốc điều trị khác nhau, sau đây Nhà thuốc AZ xin gửi tới các bạn bài viết về Thông tin thuốc Pharcavir 25mg điều trị viêm gan B: Công dụng, cách dùng, giá bán và địa chỉ mua thuốc Pharcavir 25mg giá tốt nhất Việt Nam.
Thông tin cơ bản về thuốc Pharcavir 25mg
- Thành phần chính: Tenofovir alafenamide 25mg
- Công dụng: Ức chế sự phát triển và nhân lên của vi-rút HBV từ đó điều trị bệnh vi-rút viêm gan siêu vi B mãn tính ở giai đoạn xơ gan còn bù (chưa mất chức năng gan).
- Nhà sản xuất: Công ty cổ phần dược phẩm Trung ương I – Pharbaco – Việt Nam
- Số đăng ký: VD3-29-19
- Đóng gói: Hộp 03 vỉ x 10 viên
- Dạng bào chế: Viên nén bao phim
- Nhóm thuốc: Các bệnh về gan

Thành phần của thuốc Pharcavir 25mg
- Mỗi viên nhân của thuốc Pharcavir có chứa 25mg Tenofovir alafenamide (dưới dạng Tenofovir alafenamide fumarate) và một số với tá dược: Lactose monohydrate, Cellulose vi tinh thể (E460 (i)), Croscarmelloza natri (E468), Magiê stearate (E470b).
- Màng bao phim là hỗn hợp của: Rượu polyvinyl (E1203), Titanium dioxide (E171), Macrogol (E1521), Talc (E553b), Sắt oxit màu vàng (E172).
Thuốc Pharcavir 25mg là thuốc gì? Pharcavir 25mg giá bao nhiêu?
Thuốc Pharcavir 25mg là thuốc ức chế mạnh enzym trong quá trình nhân lên và sao chép của virus viêm gan B trong cơ thể. Pharcavir kìm hãm sự nhân lên và phát triển ồ ạt các virus dẫn tới không gây ra các triệu chứng bệnh về gan của người bệnh.
Pharcavir kết hợp với các thuốc kháng retrovirus khác điều trị nhiễm virus HI-V tuýp 1 ở người lớn. Phòng ngừa lây nhiễm HIV ở người bệnh có nguy cơ lây nhiễm virus.
Thuốc Pharcavir với thành phần Tenofovir alafenamide 25mg đã được FDA hoa kỳ công nhận là thuốc mới điều trị viêm gan siêu vi B mạn tính vào năm 2016
Công dụng – Chỉ định của thuốc Pharcavir 25mg
- Thuốc Pharcavir 25 mg là thuốc ức chế mạnh enzym trong quá trình nhân lên và sao chép cúa vii-rút viêm gan B. Kì hãm sự nhân lên và phát triển ồ ạt các vi-rút dẫn tới không gây ra các triệu chứng bệnh về gan.
- Kết hợp với các thuốc kháng retrovirus khác điều trị nhiễm vi-rút HIV týp 1 ở người trưởng thành. Phòng ngừa lây nhiễm HIV ở người có nguy cơ lây nhiễm virus.
Những chú ý khi sử dụng thuốc Pharcavir:
- Thuốc không sử dụng cho bệnh nhân xơ gan mất bù
- Kiểm tra và chú ý liều lượng đối với bệnh nhân suy thận, tối loạn calci máu.
Đối tượng sử dụng thuốc Pharacvir 25mg
Hướng dẫn sử dụng thuốc Pharcavir 25mg giá bao nhiêu
Người lớn và thanh thiếu niên (từ 12 tuổi trở lên với trọng lượng cơ thể ít nhất 35 kg): một viên mỗi ngày một lần.
Ngừng điều trị có thể được xem xét như sau
• Ở những bệnh nhân dương tính với HBeAg mà không bị xơ gan, điều trị được khuyến cáo trong ít nhất 6-12 tháng sau khi huyết thanh HBe (mất HBeAg và mất DNA HBV khi phát hiện chống HBe) được xác nhận hoặc cho đến khi huyết thanh HBs hoặc cho đến khi mất hiệu quả. Đánh giá lại thường xuyên nên được thực hiện sau khi ngừng điều trị để phát hiện tái phát virus.
• Ở những bệnh nhân âm tính với HBeAg mà không bị xơ gan, điều trị nên được điều trị ít nhất cho đến khi huyết thanh HBs hoặc cho đến khi bằng chứng mất hiệu quả được chứng minh. Khi điều trị kéo dài hơn 2 năm, nên đánh giá lại thường xuyên để xác nhận rằng việc tiếp tục điều trị đã chọn vẫn phù hợp với bệnh nhân.
Liều bị bỏ lỡ
Nếu bỏ lỡ một liều và ít hơn 18 giờ kể từ thời gian thông thường, bệnh nhân nên dùng Pharcavir 25mg càng sớm càng tốt và sau đó tiếp tục lịch dùng thuốc bình thường. Nếu đã hơn 18 giờ kể từ thời gian dùng thuốc thông thường, bệnh nhân không nên dùng liều bỏ lỡ và chỉ cần tiếp tục lịch dùng thuốc bình thường.
Nếu bệnh nhân nôn trong vòng 1 giờ sau khi dùng Pharcavir 25mg bệnh nhân nên uống một viên thuốc khác. Nếu bệnh nhân nôn hơn 1 giờ sau khi dùng Pharcavir 25mg, bệnh nhân không cần uống thêm một viên thuốc nào nữa.
Sử dụng thuốc cho đối tượng đặc biệt
Già cả
Không cần điều chỉnh liều Pharcavir 25mg ở bệnh nhân từ 65 tuổi trở lên
CKD
Không cần điều chỉnh liều Pharcavir 25mg ở người lớn hoặc thanh thiếu niên (ít nhất 12 tuổi và ít nhất 35 kg trọng lượng cơ thể) với khoảng sáng nếp nhăn ước tính (CrCl) ≥ 15 mL / phút hoặc ở bệnh nhân có CrCl <15 mL / phút đang chạy thận nhân tạo.
Vào những ngày chạy thận nhân tạo, Pharcavir 25mg nên được quản lý sau khi hoàn thành điều trị chạy thận nhân tạo
Không có khuyến cáo dùng thuốc cho bệnh nhân crcl <15 mL / phút những người không chạy thận nhân tạo
Suy gan
Không cần điều chỉnh liều Pharcavir 25mg ở bệnh nhân suy gan
Dân số nhi khoa
Sự an toàn và hiệu quả củaPharcavir 25mg ở trẻ em dưới 12 tuổi, hoặc nặng <35 kg, chưa được thiết lập. Không có dữ liệu có sẵn.
Cách dùng thuốc hiệu quả:
- Sử dụng thuốc bằng đường uống, nên uống sau khi ăn no
- Nếu quên liều trong 18 tiếng thì có thể bổ sung liều nhưng nếu gần với liều tiếp theo thì không uống 2 liều cùng một lúc tránh trường hợp quá liều.
Chống chỉ định của thuốc Pharcavir 25mg – Pharcavir 25mg giá bao nhiêu?
Thuốc Pharcavir không được sử dụng trong những trường hợp nào?
- Không sử dụng thuốc Pharcavir cho bệnh nhân mẫn cảm với thuốc
- Không sử dụng thuốc Pharcavir cho bệnh nhân dị ứng hoạt chất hay bất kì thành phần tá dược.
- Không khuyến cáo dùng thuốc cho bệnh nhân mắc các bệnh thân giai đoạn cuối và xơ gan mất bù.
Thận trọng khi sử dụng thuốc Pharcavir 25mg
- Khi bắt buộc dùng thuốc Pharcavir , bệnh nhân cần được theo dõi cẩn thận về tác dụng phụ bất thường hoặc tác dụng mạnh.
- Phản ứng quá mẫn có thể xảy ra ở những người nhạy cảm.
- Thận trọng trên những bệnh nhân có rối loạn chức năng thận và quá trình đào thải
- Duy trì được hoạt lực kháng virus tốt nhất bằng cách sử dụng thuốc đều đặn hàng ngày trong suốt quá trình điều trị, sử dụng đúng liều và đúng giờ.
- Tự ý dừng uống thuốc vì sẽ dẫn đến tình trạng bệnh của bệnh dẫn đến các biến chứng nghiêm trọng như xơ gan, ung thư gan.
- Chưa có chứng minh thuốc có bài tiết qua sữa mẹ và ảnh hưởng đến thai nhi nên cần phải cân nhắc kỹ giữa lợi ích và nguy cơ trước khi sử dụng thuốc cho các phụ nữ mang thai và cho con bú
Tương tác thuốc
Thuốc Pharcavir có tương tác với một thuốc thuộc nhóm an thần, gây ngủ, thuốc chống co giật và một số kháng sinh như: Carbamazepin, Phenobarbital, Phenytoin, Itraconazole, Ketoconazole, Rifampicin, Rifabutin,… Thuốc ảnh hưởng tới hoạt động protein kháng ung thư vú nên sử dụng thuốc cách xa P-glycoprotein (P-gp).
Tác dụng phụ khi sử dụng thuốc Pharcavir 25mg
Các tác dụng không mong muốn trong quá trình sử dụng thuốc Pharcavir trên lâm sàng được thống kê chủ yếu rối loạn tiêu hóa và rối loạn thần kinh
- Rất phổ biến: Đau đầu
- Thường gặp: Chóng mặt, đau bụng, ho, đau lưng, mệt mỏi, buồn nôn, đau khớp, tiêu chảy và khó tiêu, ALT tăng, phát ban, ngứa,…
Quá liều và xử lý
- Trong các trường hợp sử dụng thuốc Pharcavir quá liều so với liều được chỉ định, bệnh nhân phải được theo dõi chặt chẽ bằng chứng về độc tính, các triệu chứng và phản ứng của cơ thể và điều trị triệu chứng thích hợp được đưa ra.
- Nồng độ thuốc tự do trong máu lớn do sự gắn kết albumin huyết tương lỏng lẻo nên có thể dùng phương pháp thẩm tách máu với hệ số chiết xuất khoảng 54%.
Cập nhật phác đồ điều trị viêm gan B bằng thuốc kháng virus
Mục tiêu điều trị viêm gan B
Ức chế lâu dài của việc nhân rộng HBV.
– Nâng cao chất lượng cuộc sống, ngăn ngừa sự tiến triển của xơ gan, HCC.
– Phòng ngừa lây truyền HBV ra cộng đồng bao gồm phòng ngừa lây truyền từ mẹ sang con.
– Phòng chống dịch VGVR B.
Nguyên tắc điều trị viêm gan B
Lựa chọn đầu tiên là chất tương tự nucleotide (NAs) đường uống. Chế độ chứa Peg-IFN chỉ nên được sử dụng trong một số trường hợp đặc biệt.
– Điều trị HBV mãn tính bằng NAs là một phương pháp điều trị lâu dài có thể kéo dài suốt đời.
– Tuân thủ.
Chuẩn bị điều trị
– Tư vấn cho bệnh nhân về các vấn đề sau:
Nhu cầu, mục tiêu và hiệu quả của liệu pháp kháng retrovirus.
+ Tầm quan trọng của việc tuân thủ điều trị (cách uống thuốc, uống thuốc đúng giờ, theo dõi khám đúng giờ…).
+ Các xét nghiệm cần thiết để chẩn đoán, theo dõi và đánh giá điều trị.
+ Điều trị lâu dài, có thể suốt đời (đối với NAs).
+ Tác dụng không mong muốn của thuốc.
+ Biến chứng HCC có thể xảy ra, ngay cả trong quá trình điều trị kháng retrovirus, đặc biệt là các trường hợp xơ gan F ≥ 3.
– Các xét nghiệm cần thực hiện trước khi điều trị:
+ Phân tích tế bào máu hoàn chỉnh (Công thức máu).
+ AST, ALT, serum creatinine.
+ Các xét nghiệm đánh giá chức năng gan khi cần thiết như bilirubin, albumin, tỷ lệ prothrombin, INR,…
+ Siêu âm bụng, AFP,…
+ Tải lượng DNA HBeAg, HBV.
+ Chống HCV.
+ Đánh giá giai đoạn xơ gan theo chỉ số APRI hoặc một trong các kỹ thuật: FibroScan, ARFI, sinh thiết gan,…
+ Nếu bệnh nhân điều trị bằng Peg-IFN cần làm thêm các xét nghiệm để đánh giá chức năng tuyến giáp (TSH, FT3, FT4), điện tâm đồ,…
+ Các xét nghiệm khác theo chỉ định lâm sàng.
Chỉ định điều trị kháng vi-rút
Dựa trên sự kết hợp của 3 yếu tố: mức ALT, tải DNA HBV và mức độ xơ gan.
Đối với trường hợp xơ gan được bồi thường, mất bù
Chẩn đoán dựa trên các triệu chứng lâm sàng và / hoặc đánh giá xơ gan là F4 bằng các phương pháp không xâm lấn hoặc bằng sinh thiết
Điều trị khi tải DNA HBV vượt quá ngưỡng bất kể mức ALT và trạng thái HBeAg.
Đối với các trường hợp không xơ gan
– Điều trị nhiễm HBV mạn tính cho bệnh nhân khi đáp ứng cả hai tiêu chí:
Tổn thương tế bào gan
– AST, ALT > 2 lần ULN và/hoặc
– Xơ gan F 2 (Phụ lục 2)
Virus đang sinh sôi nảy nở
– DNA HBV 20.000 IU/mL (≥ 105 bản/mL) nếu HBeAg dương tính
– DNA HBV > 2.000 IU/mL (≥ 104 bản sao/mL) nếu HBeAg âm tính
– Đối với các trường hợp không đáp ứng hai tiêu chí trên, chỉ định điều trị khi có một trong các tiêu chí sau:
+ Trên 30 tuổi có ALT dai dẳng cao hơn ULN (ít nhất 3 được ghi nhận trong 24-48 tuần) và DNA HBV > 20.000 IU / ml, bất kể tình trạng HBeAg.
Tiền sử gia đình mắc HCC hoặc xơ gan
+ Có các biểu hiện ngoại trú như viêm cầu thận, viêm đa khớp, cryoglobulinemia, viêm đa khớp nốt…
Tái phát sau khi ngừng điều trị chống HBV
Các thuốc kháng virus được chỉ định điều trị
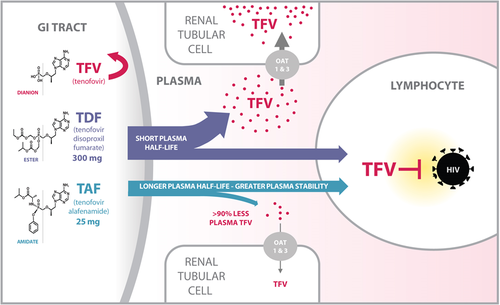
1.Tenofovir disoproxil fumarate* (TDF)
Liều dùng: 300 mg/ngày
– Đối với người có suy thận: điều chỉnh liều theo mức lọc cầu thận
Đối tượng: Trẻ e trên ≥ 12 tuổi và cân nặng ≥ 35 kg: liều lượng như người lớn
Tác dụng phụ (ADR): Bệnh thận, hội chứng Fanconi, hội chứng loãng xương, nhiễm toan lactic
Các thuốc cụ thể như: thuốc Viread 300mg, Thuốc Ricovir 300mg, Thuốc Tefosatd T300
2.Entecavir (ETV)
Liều dùng: – 0,5 mg/ngày (1 mg/ngày nếu người bệnh từng sử dụng lamivudine hoặc có xơ gan mất bù)
– Đối với người có suy thận: điều chỉnh liều theo mức lọc cầu thận (Phụ lục 4)
Trẻ ≥ 2 tuổi: tính liều theo cân nặng:
– 10-11 kg: 0,15 mg (3 mL)
– > 11-14 kg: 0,2 mg (4 mL)
– > 14-17 kg: 0,25 mg (5 mL)
– > 17-20 kg: 0,3 mg (6 mL)
– > 20-23 kg: 0,35 mg (7 mL)
– > 23-26 kg: 0,4 mg (8 mL)
– > 26-30 kg: 0,45 mg (9 mL)
– > 30kg: 0,5 mg (10 mL dung dịch uống hoặc 1 viên 0,5 mg)
ADR: Nhiễm toan lactic
Các thuốc cụ thể: Thuốc Baraclude 0.5mg, Thuốc Hepariv 0.5mg,
3. Tenofovir alafenamide** (TAF)
– 25 mg/ngày
– Không cần giảm liều đối với các trường hợp suy thận nhẹ, vừa và nặng, hoặc chạy thận.
Trẻ ≥ 12 tuổi: liều như người lớn*
Nhiễm toan lactic, không chỉ định cho trường hợp xơ gan mất bù
Các thuốc cụ thể: Thuốc Hepbest 25mg, Thuốc Pharcavir 25mg, Thuốc Vemlidy 25mg
Thuốc Pharcavir 25mg giá bao nhiêu?
Thuốc Pharcavir 25mg giá bao nhiêu? Thuốc pharcavir được sản xuất bởi công ty cổ phần dược phẩm trung ương 1 – pharbaco central pharmaceutical JSC – Hà Nội thuộc nhóm thuốc điều trị viêm gan siêu vi B mãn tính. Thuốc Pharcavir 25 mg được bán tại các bệnh viện với nhà thuốc do chính sách giá khác nhau. Giá thuốc Pharcavir 25 mg có thể biến động tùy thuộc vào từng thời điểm.
Theo Nhà thuốc AZ tham khảo được giá bán thuốc Pharcavir hiện nay tại bệnh viện từ 680.000 đồng- 750.000 đồng 1 hộp 30 viên. Giá bán lẻ thuốc Pharcavir 25mg tại các nhà thuốc lớn ở Hà Nội, Hồ Chí Minh từ 650.000 đồng – 750.000 đồng 1 hộp.
LH 0929 620 660 để được tư vấn thuốc Pharcavir 25mg giá bao nhiêu, giá bán thuốc Pharcavir 25 mg rẻ nhất, nhiều chương trình ưu đãi hoặc xem tại website: https://nhathuocaz.com.vn. Chúng tôi cam kết bán và tư vấn thuốc Pharcavir 25mg nhập khẩu chính hãng, giá bán Pharcavir 25 mg rẻ nhất.

Mua thuốc Pharcavir 25mg ở đâu uy tín Hà Nội, HCM
Mua thuốc Pharcavir 25mg ở đâu? Thuốc Pharcavir 25mg hiện nay đã được phân phối đến các bệnh viện lớn như: Sở y tế Tỉnh Đồng Nai, Sở y tế Tỉnh Nam Định, Sở y tế thành phố Hồ Chí Minh, Bệnh viện Huyện Củ Chi, bệnh nhân cần cân nhắc nhà thuốc để mua thuốc uy tín chất lượng để tránh mua phải hàng giả, hành nhái dẫn đến tiền mất tật mang lại ảnh hưởng đến kết quả cũng như thời gian vàng của quá trình điều trị. Sau đây, Nhathuocaz.com.vn xin giới thiệu một số các địa chỉ (Hiệu thuốc, Nhà thuốc, Công ty Dược) cung cấp thuốc Pharcavir 25mg chính hãng, uy tín:
Bạn có thể mua thuốc Pharcavir 25mg chính hãng tại các cơ sở nhà thuốc AZ trên toàn quốc cũng như trên trang web online của nhà thuốc.
*Văn phòng đại diện:
Cơ sở 1: Trung tâm Phân phối thuốc, số 85 Vũ Trọng Phụng, Thanh Xuân Trung, Thanh Xuân, Hà Nội.
Cơ sở 2: Số 7 ngõ 58 Vũ Trọng Phụng, Thanh Xuân Trung, Thanh Xuân, Hà Nội địa chỉ tại đây
https://g.page/r/CTNkPnn7vyrBEA0
Cơ sở 3: Chung cư Ecogreen City, Số 286 Nguyễn Xiển, Tân Triều, Thanh Trì, Hà Nội địa chỉ tại đây
*Hệ thống nhà thuốc AZ
- Cơ sở 1: Số 201 Phùng Hưng, P Hữu Nghị, Tp Hòa Bình (Gần chợ Tân Thành)
- Cơ sở 2: Ngã Ba Xưa, Xuất Hóa, Lạc Sơn, Hòa Bình (Hiệu thuốc Lê Thị Hải)
- Cơ sở 3: Số 7 ngõ 58 Vũ Trọng Phụng, Thanh Xuân Trung, Thanh Xuân, Hà Nội
- Cơ sở 4: Phố Lốc Mới, TT Vụ Bản, Lạc Sơn, Hòa Bình (Cổng Bệnh viện huyện Lạc Sơn)
- Cơ sở 5: Chợ Ốc, Đồng Tâm, Thượng Cốc, Lạc Sơn, Hoà Bình
* Nếu bệnh nhân tìm và muốn mua các loại thuốc kê đơn, thuốc đặc trị khó tìm hoặc khi địa chỉ nhà ở xa các bệnh viện trên và cần mua thuốc. Chúng tôi có dịch vụ cung cấp đủ các loại thuốc quý khách cần, quý khách cần mua thuốc phải có đơn thuốc của bác sỹ. Nhà thuốc AZ xin hướng dẫn cách mua thuốc theo đơn tại Bệnh Viện: Tại đây
Ở các tỉnh thành khác, Chúng tôi có dịch vụ hỗ trợ quý khách mua thuốc Pharcavir 25mg chính hãng, ship thuốc COD qua các đơn vị vận chuyển uy tín như GHTK, GHN, Viettel Post, VN Post… Quý khách nhận thuốc, kiểm tra rồi mới thanh toán tiền.
Danh sách các Tỉnh, Thành Phố chúng tôi cung cấp thuốc Pharcavir 25mg: An Giang, Bà Rịa – Vũng Tàu, Bắc Giang, Bắc Kạn, Bạc Liêu, Bắc Ninh, Lâm Đồng, Lạng Sơn, Lào Cai, Long An, Nam Định, Nghệ An, Ninh Bình, Ninh Thuận, Phú Thọ, Quảng Bình, Quảng Nam, Quảng Ngãi, Quảng Ninh, Quảng Trị, Sóc Trăng, Sơn La, Tây Ninh, Thái Bình, Thái Nguyên, Gia Lai, Hà Giang, Hà Nam, Hà Tĩnh, Hải Dương, Hậu Giang, Hòa Bình, Hưng Yên, Khánh Hòa, Kiên Giang, , Thanh Hóa, Thừa Thiên Huế, Tiền Giang, Trà Vinh, Tuyên Quang, Vĩnh Long, Vĩnh Phúc, Yên Bái, Phú Yên, Cần Thơ, Đà Nẵng, Hải Phòng, Hà Nội, TP HCM, Bến Tre, Bình Định, Bình Dương, Bình Phước, Bình Thuận, Cà Mau, Cao Bằng, Đắk Lắk, Đắk Nông, Điện Biên, Đồng Nai, Đồng Tháp, Kon Tum, Lai Châu. Các tỉnh thành này bạn chỉ cần liên hệ số 0929.620.660 để được nhận thuốc tại nhà.
Đối với các quận huyện của Thủ đô Hà Nội và Thành phố Hồ Chí Minh chúng tôi có dịch vụ giao hàng nhanh trong vòng 2 tiếng. Danh sách các Quận huyện mà chúng tôi có dịch vụ cung cấp thuốc Pharcavir 25mg Quận Ba Đình, Quận Hoàn Kiếm, Quận Hai Bà Trưng, Quận Đống Đa, Quận Tây Hồ, Quận Cầu Giấy, Quận Thanh Xuân, Quận Hoàng Mai, Huyện Hoài Đức, Huyện Thanh Oai, Huyện Mỹ Đức, Huyện Ứng Hòa, Huyện Thường Tín, Huyện Phú Xuyên, Huyện Mê Linh, Quận Nam Từ Liêm, Quận Long Biên, Quận Bắc Từ Liêm, Huyện Thanh Trì, Huyện Gia Lâm, Huyện Đông Anh, Huyện Sóc Sơn, Quận Hà Đông, Thị xã Sơn Tây, Huyện Ba Vì, Huyện Phúc Thọ, Huyện Thạch Thất, Huyện Quốc Oai, Huyện Chương Mỹ, Huyện Đan Phượng: Liên hệ 0929.620.660 để được Ds Đại học Dược Hà Nội tư vấn sử dụng thuốc Pharcavir 25mg chính hãng, an toàn, hiệu quả.
Sản phẩm tương tự thuốc Pharcavir 25 mg
Ngoài ra, chúng tôi còn có các thuốc có thành phần Tenofovir alafenamide 25mg tương tự thuốc Pharcavir 25mg như:
- Thuốc Vemlidy 25 mg (Hộp 30 viên) – Gilead Sciences Ireland UC – Ai Len
- Thuốc Hepbest 25mg (Hộp 30 viên) – Công ty Mylan – Ấn Độ
- Thuốc Tafsafe 25mg (Hộp 30 viên) Atra Pharmaceuticals Limited – Ấn Độ
Dược lực học và dược động học của thuốc Pharcavir 25mg
Dược lực học
- Tenofovir alafenamide là một tiền chất nhờ các chất vận chuyển hấp thu ở gan, khuếch tán thụ động và xâm nhập vào tế bào gan nguyên phát. Tenofovir alafenamide chủ yếu được carboxylesterase 1 trong tế bào gan nguyên phát thủy phân để tạo thành tenofovir. Sau đó chuyển thành chất chuyển hóa hoạt động dược lý tenofovir diphosphate nhờ quá trình phosphoryl hóa. Tenofovir diphosphate ức chế sự sao chép HBV thông qua việc kết hợp với DNA virus bằng enzyme sao chép ngược HBV, dẫn đến sự chấm dứt chuỗi DNA.
- Tenofovir hoạt động đặc hiệu với virus viêm gan B và virus HIV gây suy giảm miễn dịch ở người. Tenofovir diphosphate là chất ức chế yếu men γ-DNA polymerase ở động vật có xương sống và α-DNA polymerase của động vật có vú.
Dược động học
- Hấp thu: Hoạt chất Tenofovir alafenamide ở dạng muối được hấp thu nhanh và chuyển hóa thành chất có hoạt lực tenofovir. Sau 1 đến 2 giờ là thuốc đạt nồng độ đỉnh trong huyết tương. Độ hấp thu phụ thuộc vào thực phẩm ví dụ như dùng bữa ăn giàu chất béo trong khi uống thuốc sẽ tăng sinh khả dụng của thuốc.
- Phân phối: Thuốc được phân phối rộng rãi trong các mô, đặc biệt ở thận và gan. Nồng độ thuốc tự do trong cơ thể lớn vì sự liên kết với protein huyết tương thấp hơn 1% và với protein huyết thanh khoảng 7%.
- Chuyển hóa: Tenofovir alafenamide được chuyển hóa bởi cathepsin A trong các tế bào đơn nhân máu ngoại vi và nhờ carboxylesterase-1 trong tế bào gan tạo thành tenofovir. Trong phòng thí nghiệm, muối tenofovir alafenamide bị thủy phân trong các tế bào để tạo thành tenofovir (chất chuyển hóa chính), được phosphoryl hóa thành chất chuyển hóa hoạt động, tenofovir diphosphate.
- Thải trừ: 12-18 giờ là thời gian bán thải của thuốc. Quá trình bài tiết Tenofovir alafenamide <1% trong nước tiểu. Phần lớn bài tiết ở dạng sau chuyển hóa được bài tiết qua ống thận và cầu thận, hoặc loại bằng thẩm phân máu.
Bài viết chỉ mang tính chất chia sẻ thông tin, quý khách hàng không tự ý sử dụng thuốc khi chưa có sự chỉ định của bác sĩ chuyên khoa.
Nếu còn thắc mắc về bất cứ thuốc điều trị viêm gan B hay về thuốc Pharcavir 25mg như: Thuốc Pharcavir 25mg giá bao nhiêu tiền? Mua thuốc Pharcavir 25mg ở đâu uy tín? Thuốc Pharcavir 25mg xách tay chính hãng giá bao nhiêu? Thuốc Pharcavir 25mg có tác dụng phụ là gì? Cách phân biệt Pharcavir 25mg chính hãng và thuốc Pharcavir 25mg giả? Thuốc điều trị viêm gan B có hiệu quả, có an toàn? Vui lòng liên hệ với nhathuocaz theo số hotline 0929 620 660 để được các Dược sĩ Đại học tư vấn một cách chính xác và tận tâm nhất. Nhathuocaz.com.vn xin chân thành cảm ơn quý khách hàng đã đọc bài viết.
Bệnh viêm gan B có hại tới sức khỏe nhiều không?
Viêm gan B là một bệnh lây truyền qua đường máu gây ra bởi virus viêm gan B (HBV). Nếu không được chẩn đoán và điều trị kịp thời, viêm gan B có thể gây ra các vấn đề sức khỏe nghiêm trọng, bao gồm:
- Viêm gan mãn tính: Đây là tình trạng viêm gan kéo dài hơn 6 tháng và có thể dẫn đến xơ gan, suy giảm chức năng gan và ung thư gan.
- Ung thư gan: Người mắc viêm gan B lâu dài có nguy cơ cao bị ung thư gan so với người không mắc bệnh. Ung thư gan là một bệnh nguy hiểm và khó chữa trị.
- Suy gan: Nếu viêm gan B kéo dài, nó có thể dẫn đến sự suy giảm chức năng gan và cuối cùng là suy gan.
- Viêm màng não: Một số trường hợp nghiêm trọng của viêm gan B có thể gây ra viêm màng não.
Tình trạng dị ứng và viêm khớp: Một số bệnh nhân mắc viêm gan B có thể phát triển tình trạng dị ứng và viêm khớp.
Do đó, viêm gan B là một bệnh nguy hiểm và có hại cho sức khỏe của con người. Tuy nhiên, nếu được phát hiện sớm và điều trị kịp thời, nguy cơ phát triển các biến chứng có thể giảm xuống đáng kể.
Thuốc Pharcavir có được lưu hành tại Việt Nam hay không? Pharcavir 25mg giá bao nhiêu?
Cục Quản lý Dược đã ban hành quyết định danh mục 5 thuốc sản xuất trong nước được cấp giấy đăng ký lưu hành tại Việt Nam.
Danh sách 5 thuốc gồm: Pharcavir, Zacutas 60, Zacutas 90, Dactasvir 30mg, Dactasvir 60mg, lần lượt có số đăng ký từ VD3-29-19 đến VD3-34-19.
Cục quản lý Dược yêu cầu cơ sở sản xuất và cơ sở đăng ký thuốc có trách nhiệm sản xuất thuốc theo đúng các hồ sơ, tài liệu đã đăng ký với Bộ Y tế và phải in số đăng ký được Bộ Y tế Việt Nam cấp lên nhãn thuốc.
Đồng thời thực hiện việc cập nhật tiêu chuẩn chất lượng của thuốc theo quy định. Cập nhật nhãn thuốc, tờ hướng dẫn sử dụng thuốc theo quy định tại Thông tư số 01/2018 trong thời hạn 6 tháng kể từ ngày ký ban hành Quyết định này, theo hình thức thay đổi, bổ sung giấy đăng ký lưu hành thuốc quy định tại Thông tư số 32/2018/TT-BYT ngày 12/11/2018 của Bộ trưởng Bộ Y tế quy định việc đăng ký lưu hành thuốc, nguyên liệu làm thuốc.
Đối với thuốc Pharcavir chứa hoạt chất tenofovir alafenamide fumarate (thuốc số 1 tại danh mục) phải cập nhật tờ hướng dẫn sử dụng theo tờ hướng dẫn sử dụng thuốc Vemlidy đã được Cơ quan Quản lý Dược Châu Âu (EMA) phê duyệt trong thời hạn 03 tháng kể từ ngày ký ban hành Quyết định này và chỉ được sản xuất, lưu hành sau khi được Cục Quản lý Dược phê duyệt nội dung này.
Nguồn báo: https://vietnamnet.vn/them-5-thuoc-noi-nhan-giay-dang-ky-luu-hanh-602990.html
Tác giả: Ds Lê Thị Trang
Tham vấn Y khoa: Ds Phạm Quốc Hoàn