Bạch cầu ái toan Eosinophils là một trong những thành phần của bạch cầu được sản sinh từ tủy xương và là một trong những tế bào có vai trò thúc đẩy tiến trình viêm, đặc biệt các phản ứng viêm dị ứng. Do vậy, một số lượng lớn eosin có thể tích tụ trong các mô như thực quản, dạ dày, ruột non và đôi khi trong máu khi những cá nhân đó phơi nhiễm với yếu tố dị nguyên.
Các thuật ngữ viết tắt trong bài viết:
EoE: Eosinophilic esophagitis: Viêm thực quản tăng esinophil
GERD: Gastroesophageal reflux disease: Bệnh lý viêm thực quản trào ngược
IL: Interleukin: yếu tố Interleukin
PPI: Proton pump inhibitor: Thuốc ức chế bơm Proton
PPI-REE: Proton pump inhibitor-responsive esophagal: bệnh lý viêm thực quản đáp ứng thuốc ức chế bơm Proton
Eosinophilia: bạch cầu ái toan
VTQBCAT: viêm thực quản bạch cầu ái toan
Khuyến cáo của Hội Tiêu hóa Mỹ năm 2013 đã nhấn mạnh nếu tăng BCAT tìm thấy ở thực quản cần đặt ra 3 khả năng: VTQTCAT, GERD và tăng BCAT thư quản đáp ứng với PPI (PPLREE).
Các hướng dẫn cập nhật vào năm 2011 đã mô tả một kiểu hình bệnh lý mới, tăng bạch cầu ái toan thực quản đáp ứng với chất ức chế bơm proton (PPI-REE), đề cập đến những bệnh nhân dường như có EoE trên lâm sàng, nhưng đã thuyên giảm hoàn toàn sau khi điều trị bằng PPI. Hiện tại,PPI-REE phải được loại trừ chính thức trước khi chẩn đoán EoE, vì 30-40% bệnh nhân nghi ngờ EoE cuối cùng được chẩn đoán với PPI-REE. Điều thú vị là PPI-REE và EoE vẫn không thể phân biệt được dựa trên các phát hiện lâm sàng, nội soi và mô học, theo dõi pH thực quản và đo lường các dấu hiệu mô và cytokine liên quan đến viêm bạch cầu ái toan, khả năng ức chế axit của liệu pháp PPI, đang trở nên lỗi thời. Ngày càng có nhiều bằng chứng cho thấy PPI-REE không thể phân biệt được về mặt di truyền và kiểu hình với EoE và liệu pháp PPI đơn thuần có thể đảo ngược hoàn toàn chứng viêm dị ứng. Như vậy, PPI-REE có thể tạo thành một kiểu phụ của EoE và liệu pháp PPI có thể là bước điều trị đầu tiên và chế độ ăn kiêng / steroid có thể đại diện cho liệu pháp nâng cao. Có thể, thuật ngữ PPI-REE sẽ sớm được thay thế bằng EoE đáp ứng PPI. Cơ chế tại sao một số bệnh nhân đáp ứng với liệu pháp PPI (PPI-REE) trong khi những người khác thì không (EoE), vẫn còn được làm sáng tỏ.
1. Sinh bệnh học của PPI-REE
Vì PPI-REE không thể phân biệt được về mặt lâm sàng với EoE, và vì việc tiếp xúc với axit thực quản không giải thích được phản ứng PPI một cách đáng tin cậy, liệu cơ chế bệnh sinh của PPI-REE có tương tự như EoE không? EoE là một tình trạng qua trung gian miễn dịch, trong đó ở các cá thể có khuynh hướng di truyền, các kháng nguyên thực phẩm hoặc môi trường kích hoạt phản ứng qua trung gian T-helper (Th2) loại 2 mặc dù các cytokine như interleukin (IL) -4, IL-5 và IL-13, kích thích thực quản sản xuất eotaxin-3 (một chất hóa trị bạch cầu ái toan). Tiếp theo là tuyển dụng và kích hoạt bạch cầu ái toan trong niêm mạc thực quản. Các chất trung gian khác liên quan đến sinh bệnh học của EoE bao gồm yếu tố tăng trưởng biến đổi-β1, yếu tố tăng trưởng nguyên bào sợi và lymphopoietin mô đệm tuyến ức. Eotaxin-3 trong thực quản là yếu tố chính thúc đẩy quá trình hóa học của bạch cầu ái toan, kích hoạt và sau đó giải phóng các hạt nội bào như protein cơ bản chính (MBP) và các chất trung gian gây viêm khác. Các cuộc điều tra trước cho thấy MBP và eotaxin-3 được điều chỉnh tăng đáng kể trong biểu mô thực quản của bệnh nhân EoE so với nhóm chứng GERD và có thể được sử dụng trên lâm sàng để dự đoán tình trạng EoE. Việc nhuộm tế bào mast để tìm tryptase cũng đã thành công trong việc phân biệt EoE với GERD.
Các nghiên cứu gần đây đã chỉ ra rằng những dấu hiệu tương tự này cũng tăng lên trong PPI-REE, và trong khi có sự khác biệt giữa EoE và GERD, không có sự khác biệt giữa EoE và PPI-REE . Trong một nghiên cứu tiền cứu trên 23 bệnh nhân có PPI-REE, 50 bệnh nhân có EoE và 123 đối chứng, nhuộm mô miễn dịch sinh thiết thực quản tìm MBP, eotaxin-3 và tryptase tế bào mast cho thấy mức độ cao của cả ba dấu ấn trong cả EoE và PPI-REE. Sau một thử nghiệm PPI, các dấu hiệu này trở lại bình thường trong PPI-REE, nhưng vẫn tăng ở các đối tượng EoE. Một nghiên cứu tiền cứu tương tự của Molina-Infante và cộng sự so sánh bệnh nhân EoE và PPI-REE cho thấy không có sự khác biệt đáng kể về mức độ biểu hiện gen của eotaxin-3 và IL-13 trong toàn bộ thực quản và của IL-5 ở thực quản xa. Mức độ biểu hiện của cả ba cytokine cũng giảm sau khi điều trị PPI ở nhóm PPI-REE. Do đó, dữ liệu miễn dịch học hiện có so sánh EoE và PPI-REE cho thấy rằng các yếu tố viêm tương tự có thể liên quan đến cơ chế bệnh sinh của chúng.
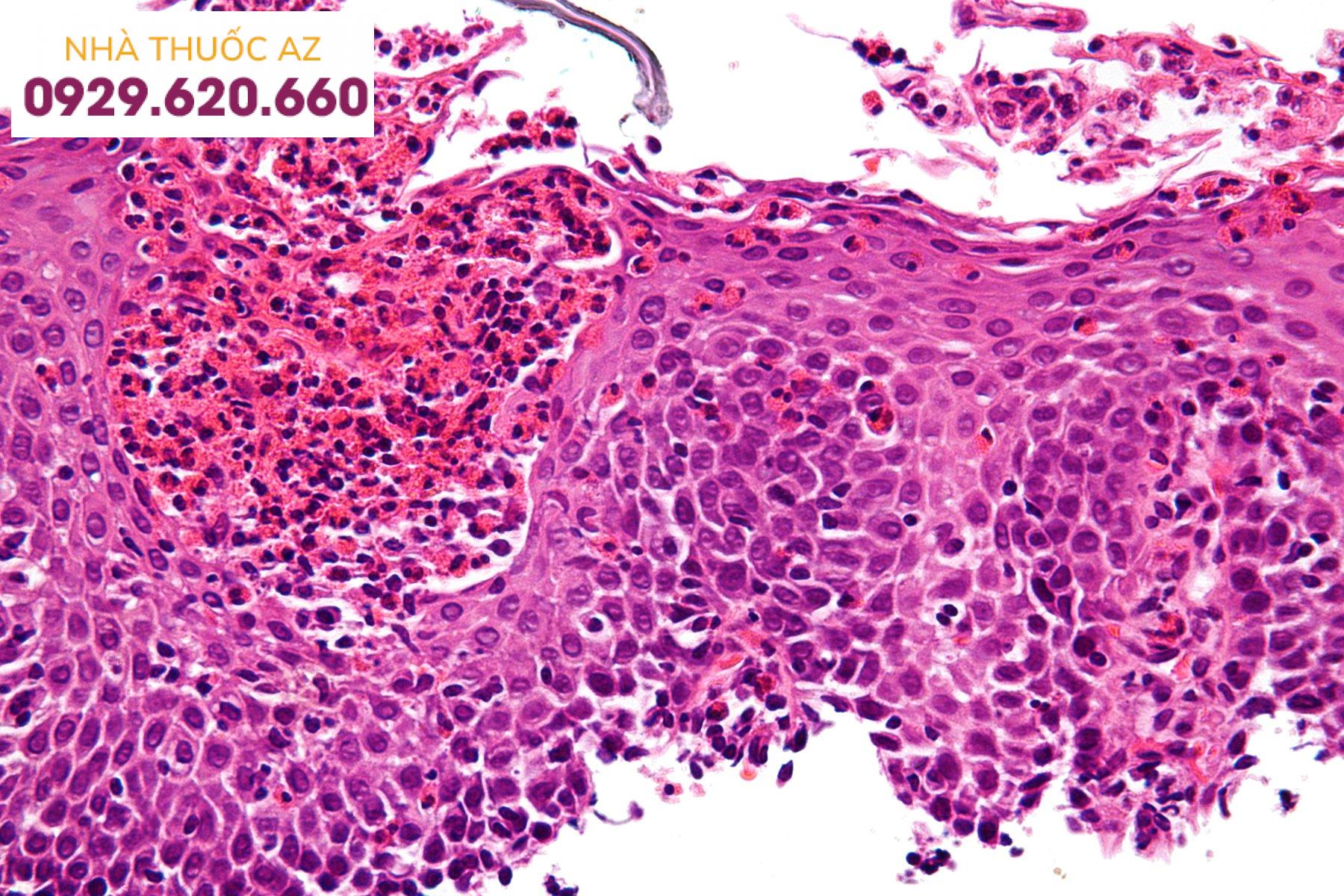
Hình ảnh hiển vi cho thấy viêm thực quản tăng bạch cầu ái toan.
2. Biểu hiện di truyền trong PPI-REE
Vì EoE và PPI-REE không thể phân biệt được về mặt lâm sàng và mô học, các dấu ấn sinh học phân tử hữu ích sẽ được mong muốn. Bảng chẩn đoán EoE (EDP) là một xét nghiệm di truyền bao gồm 94 gen được biểu hiện khác biệt trong EoE và có thể xác định một cách đáng tin cậy bệnh nhân EoE. Khi EDP lần đầu tiên được đánh giá trong PPI-REE, mô hình biểu hiện gen của bệnh nhân PPI-REE trước khi sử dụng PPI rất giống với mô hình trong EoE và bao gồm các gen chính liên quan đến EoE cho quá trình hóa học bạch cầu ái toan (CCL26), gen tế bào mast (CPA3 và TPSAB2), dấu hiệu viêm Th2, gen hàng rào biểu mô và dấu hiệu xơ hóa mô. Hơn nữa, dấu hiệu di truyền này trong PPI-REE đã đảo ngược sau khi điều trị PPI theo cách tương tự như những gì được thấy ở bệnh nhân EoE sau khi ăn kiêng hoặc điều trị steroid. Ngược lại, PPI không đảo ngược các đặc điểm phân tử trong EoE.
Mặc dù nghiên cứu nói trên cho thấy phần lớn các transcriptomes trùng lặp giữa bệnh nhân PPI-REE và những người có EoE, các nhà điều tra đã tìm thấy một số khác biệt đáng kể giữa bệnh nhân EoE và bệnh nhân PPI-REE (trước khi thử nghiệm PPI của họ) trong biểu hiện cơ bản của một nhóm 10 gen. Một gen, KCNJ2, đã vượt qua tỷ lệ phát hiện sai và đã được nghiên cứu thêm. KCNJ2 được biểu hiện ở mức cao trong nhóm EoE, nhưng ở mức thấp ở nhóm chứng bình thường và bệnh nhân PPI-REE, và có thể dự đoán PPI-REE so với EoE với độ nhạy 72% và độ đặc hiệu 72%. KCNJ2 mã hóa kênh kali Kir2.1, có nhiều trong niêm mạc đường tiêu hóa và đồng địa hóa với bơm H1-K1 ATPase / proton. Vai trò của Kir2.1 trong bài tiết axit có thể giải thích phản ứng PPI và các nghiên cứu bổ sung đang được tiến hành để đánh giá tiện ích lâm sàng của chất chỉ điểm này. Những phát hiện mới này có tính khiêu khích và hỗ trợ cơ chế bệnh sinh qua trung gian miễn dịch được chia sẻ tiềm năng giữa EoE và PPI-REE.
3. Cơ chế phản ứng PPI trong PPI-REE
Vì có thể có chung cơ chế bệnh sinh giữa EoE và PPI-REE, các cơ chế làm cơ sở cho phản ứng PPI trong tăng bạch cầu ái toan thực quản cũng đã được nghiên cứu gần đây. Với mối liên quan giữa GERD và bạch cầu ái toan, một giả thuyết cho rằng phản ứng PPI trong PPI-REE là thông qua cơ chế giảm axit, điều trị GERD cơ bản không rõ ràng về mặt lâm sàng. Ngay cả khi không có triệu chứng, tiếp xúc với axit từ GERD có thể gây tổn thương biểu mô thực quản, cho phép sự xâm nhập của các kháng nguyên dị ứng gây ra phản ứng tăng bạch cầu ái toan trong niêm mạc. Một nghiên cứu tiền cứu đã so sánh tính toàn vẹn của hàng rào ở 8 bệnh nhân PPI-REE và 8 bệnh nhân EoE, được đo bằng không gian nội bào giãn ra, trở kháng mô điện, điện trở xuyên biểu mô và thông lượng phân tử. Các nhà điều tra phát hiện ra rằng, trước khi thử nghiệm PPI, chức năng rào cản đã giảm ở cả PPI-REE và EoE, nhưng chỉ được phục hồi trong nhóm PPI-REE sau thử nghiệm PPI. Tuy nhiên, cần phải làm thêm để làm sáng tỏ các cơ chế của chức năng rào cản được cải thiện này.
Một cơ chế tiềm năng mới khác của PPI-REE dựa trên tác dụng chống viêm của PPIs. Hai nghiên cứu gần đây đã chứng minh làm giảm chất trung gian liên quan đến Th2 trong các dòng tế bào EoE được điều trị bằng omeprazole, tương tự như phát hiện trong một nghiên cứu về bệnh hen suyễn ở mô hình phổi chó. Omeprazole chặn cả bài tiết eotaxin-3 do IL-4- và IL-13 kích thích từ hai dòng tế bào vảy EoE trong một hệ thống thí nghiệm không có axit. Đây là một minh chứng mạnh mẽ cho một bằng chứng về nguyên tắc rằng PPI có thể có cơ chế chống viêm trong tăng bạch cầu ái toan thực quản. Hơn nữa, những nghiên cứu này cho thấy rằng cơ chế mà omeprazole ngăn chặn sự tiết eotaxin-3 do cytokine kích thích là bằng cách ngăn STAT6 liên kết với vùng khởi động của gen eotaxin-3. Các nhà nghiên cứu này cũng mô tả hiệu ứng PPI khác biệt theo vị trí thực quản trong các mẫu sinh thiết lâm sàng, với sự ức chế nổi bật hơn của eotaxin-3 ở thực quản gần. Điều thú vị là không giống như sự bài tiết eotaxin-3 bởi các tế bào biểu mô, sự bài tiết eotaxin-3 bởi các nguyên bào sợi không bị chặn bởi PPIs, cho thấy rằng có những quá trình bổ sung góp phần vào cơ chế bệnh sinh của EoE và PPI-REE.
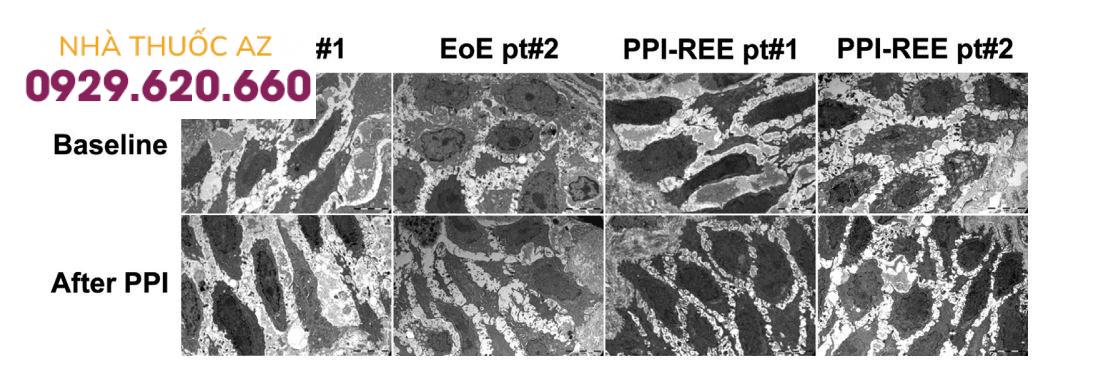
Hình ảnh hiển vi điện tử truyền qua của lớp gai đáy của bệnh phẩm sinh thiết niêm mạc thực quản cho thấy các khoảng gian bào bị giãn ra
Cơ chế thứ ba, mới bắt đầu được nghiên cứu, giải quyết sự chuyển hóa PPI khác biệt như một cơ chế tiềm năng của phản ứng PPI. Một loạt trường hợp trước đó mô tả bốn trẻ bị PPI-REE mất khả năng đáp ứng PPI (tức là chúng phát triển các triệu chứng tái phát và tăng bạch cầu ái toan thực quản), mặc dù được duy trì liều PPI ổn định và không có các yếu tố gây nhiễu khác, và cuối cùng chúng đáp ứng các tiêu chuẩn chẩn đoán cho EoE. Trong một nghiên cứu được trình bày dưới dạng tóm tắt bởi Molina-Infante và cộng sự, 72% trong số 46 bệnh nhân PPI-REE được theo dõi lâu dài có đáp ứng PPI bền vững. Tám bệnh nhân tái phát với việc giảm liều PPI của họ sau đó đáp ứng với việc tăng liều PPI, và cũng có kiểu hình chuyển hóa PPI nhanh chóng khi xét nghiệm men CYP450. Trong khi tất cả các cơ chế tiềm năng này của phản ứng PPI đòi hỏi phải nghiên cứu thêm, chúng chỉ ra một số cách đa dạng và không phụ thuộc vào axit mà PPI có thể làm giảm bạch cầu ái toan thực quản.
Để biết thêm các thông tin chi tiết, vui lòng liên hệ với Nhà thuốc AZ theo số hotline 0929 620 660 hoặc truy cập vào website: https://nhathuocaz.com.vn